Beim Seebeck-Effekt (https://stoppi-homemade-physics.de/seebeck-effekt/) haben wir schon die sog. thermoelektrische Spannungsreihe kennengelernt. Bringt man die beiden Kontaktstellen von zwei verschiedenen Metalldrähten auf unterschiedliche Temperatur, so misst man eine Thermospannung. Diese hängt von der Metallpaarung ab und vom Temperaturunterschied.

Bei der elektrochemischen Spannungsreihe steckt man z.B. zwei verschiedene Metallplatten in eine Zitrone und kann dann zwischen den beiden Platten eine elektrische Spannung messen. Diese hängt nur von der verwendeten Metallpaarung ab. Warum ist dies so?

Tauchen zwei verschiedene Metallplatten in einen Elektrolyten, so gehen die Metalle unterschiedlich stark in Lösung. Das edlere Metall geht weniger in Lösung, das unedlere mehr. Dadurch bleiben beim edleren Metall weniger Elektronen in der Platte zurück und sie bildet die sog. Anode (positiver Pol). Beim unendleren Metall ist es genau anders. Hier bleiben durch das stärker in Lösung gehen mehr Elektronen zurück und dort befindet sich dann der negative Pol (Kathode). Bei der Paarung Kupfer-Zink ist etwa Kupfer das edlere Metall und bildet demnach die Anode aus.
Geht man von einem Normpotential 0V für ein bestimmtes Metall aus. konkret Wasserstoff, so kann man alle anderen Metalle dann in einer Spannungsreihe von unedel (negatives Potential) bis edel (positives Potential) ordnen:

Quelle: https://goldschmiede-plaar.de/2014/02/22/elektrochemische-spannungsreihe/
Für dieses Experiment benötigt man also nur eine Zitrone und verschiedene Metallplatten. Diese habe ich auf ebay.com gekauft. Mit dabei ist Zink, Kupfer, Titan, Aluminium, Blei, Nickel, Wolfram, Eisen und Silber.



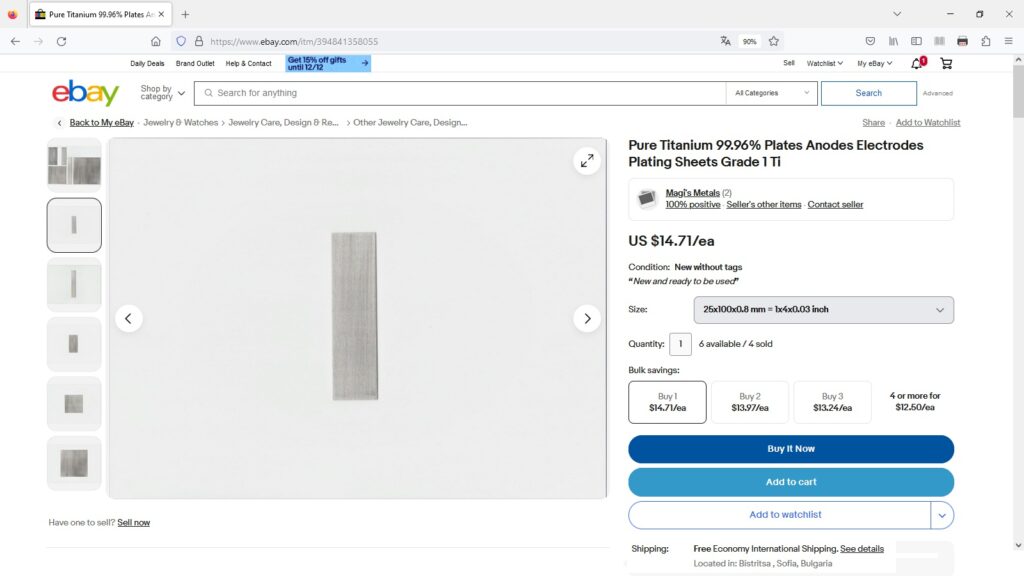

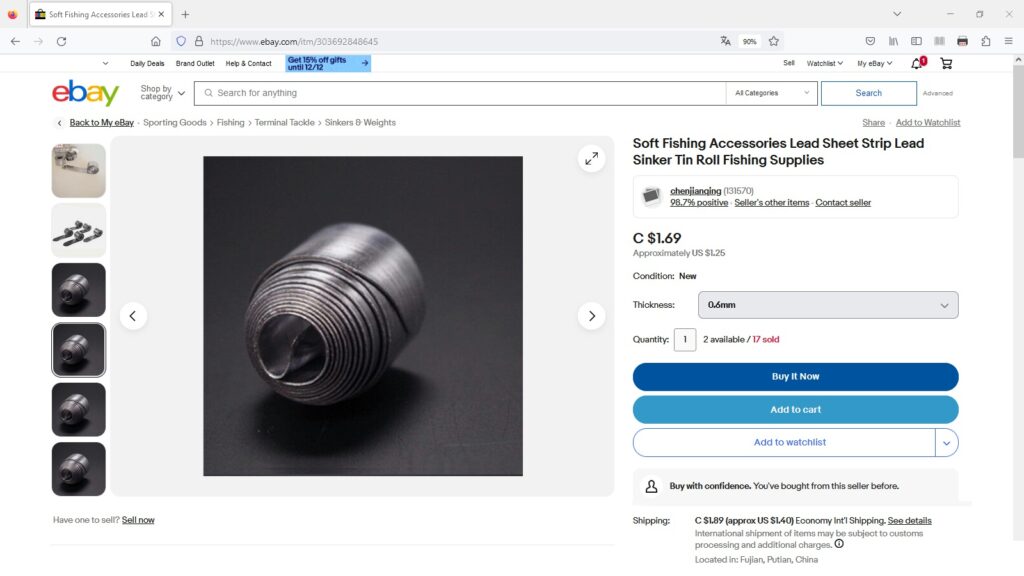




Zur Aufnahme der elektrochemischen Spannungsreihe habe ich Blei als Bezugspotential gewählt, weil es auch in der Spannungsreihe nahe bei 0V liegt. Dann habe ich sämtliche Metalle in Kombination mit Blei durchprobiert und die jeweiligen Spannungen notiert.

Kombination Zink-Blei:


Kombination Eisen-Blei:


Kombination Titan-Blei: Hier sollte man eigentlich eine Spannung von –1.63 – (–0.13) = –1.5 V erhalten. Meine Messung ergab allerdings eine Spannung von nur rund +0.14 V.


Kombination Aluminium-Blei:


Kombination Nickel-Blei:


Kombination Kupfer-Blei:


Kombination Silber-Blei:


Kombination Wolfram-Blei:


Teilweise weichen die erhaltenen Spannungen erheblich von den Sollwerten laut elektrochemischer Spannungsreihe ab. Dies aber sicherlich auch deshalb, weil der Aufbau mit der Zitrone keiner „Normzelle“ entspricht.

Kombiniert man dasselbe Metall, so müsste die Spannung bei 0V liegen. Bei der Paarung Kupfer-Kupfer konnte ich in der Tat wie zu erwarten nahezu 0V messen:



Wählt man nun zwei beliebige, verschiedene Metalle aus, so müsste sich eine Spannung ergeben, welche der Differenz der beiden elektrochemischen Potentiale entspricht. Bei der Kombination Kupfer-Zink erwartet man deshalb +0.34 – (–0.76) = +1.1 V. Auch dies konnte durch eine Messung annähernd bestätigt werden:



Wie immer abschließend das Youtube-Video:
Voltasche Säule

Bildquelle: https://commons.wikimedia.org/wiki/File:Alessandro_Volta.jpeg#/media/Datei:Alessandro_Volta.jpeg, https://www.anthroposophie.net/bibliothek/nawi/physik/volta/bib_volta.htm</a>, Gemeinfrei, „https://commons.wikimedia.org/w/index.php?curid=1678917“
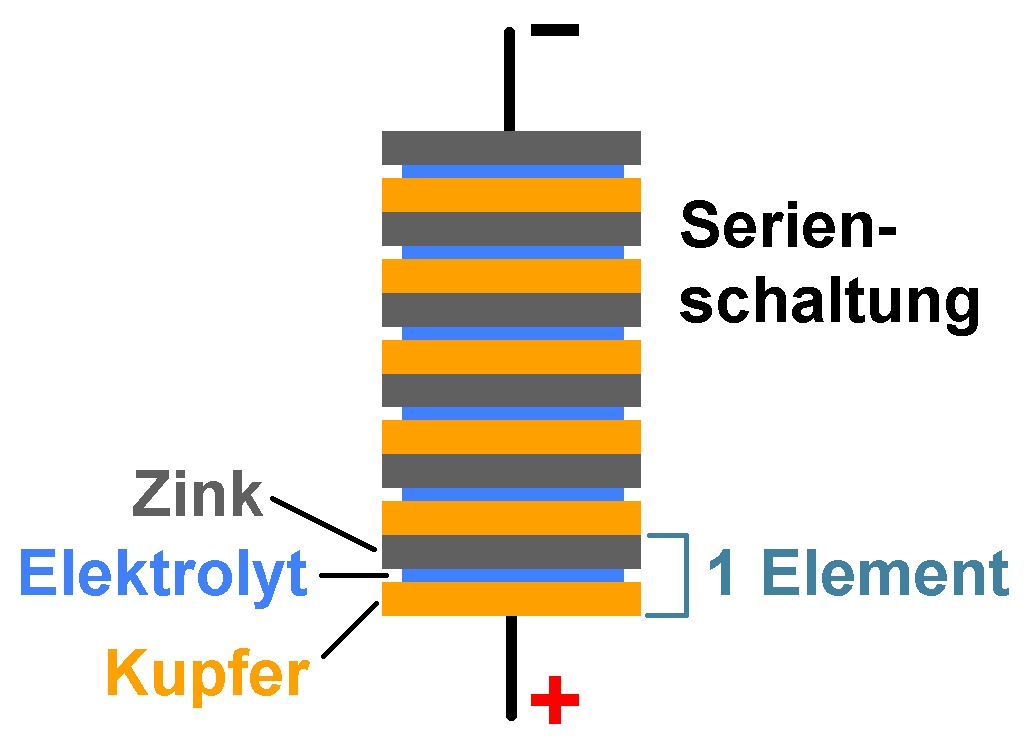
Die Volta’sche Säule oder auch Voltasäule ist die erste elektrische Batterie, die eine praktische Bedeutung als Stromquelle erlangte. Sie wurde von Alessandro Volta um 1799 entwickelt und der Royal Society im Jahr 1800 in London vorgestellt. Sie besteht aus vielen übereinander geschichteten Kupfer- und Zinkplättchen, zwischen denen sich in bestimmter regelmäßiger Folge elektrolytgetränkte Papp- oder Lederstücke befinden.
Ich verwende für meine Voltasche Säule Kupfer- (in Form von 2 cent Münzen) und Zinkmünzen (alte 5 Groschen Münzen). Letztere habe ich für nur 10 cent pro Stück über http://www.willhaben.at gekauft:
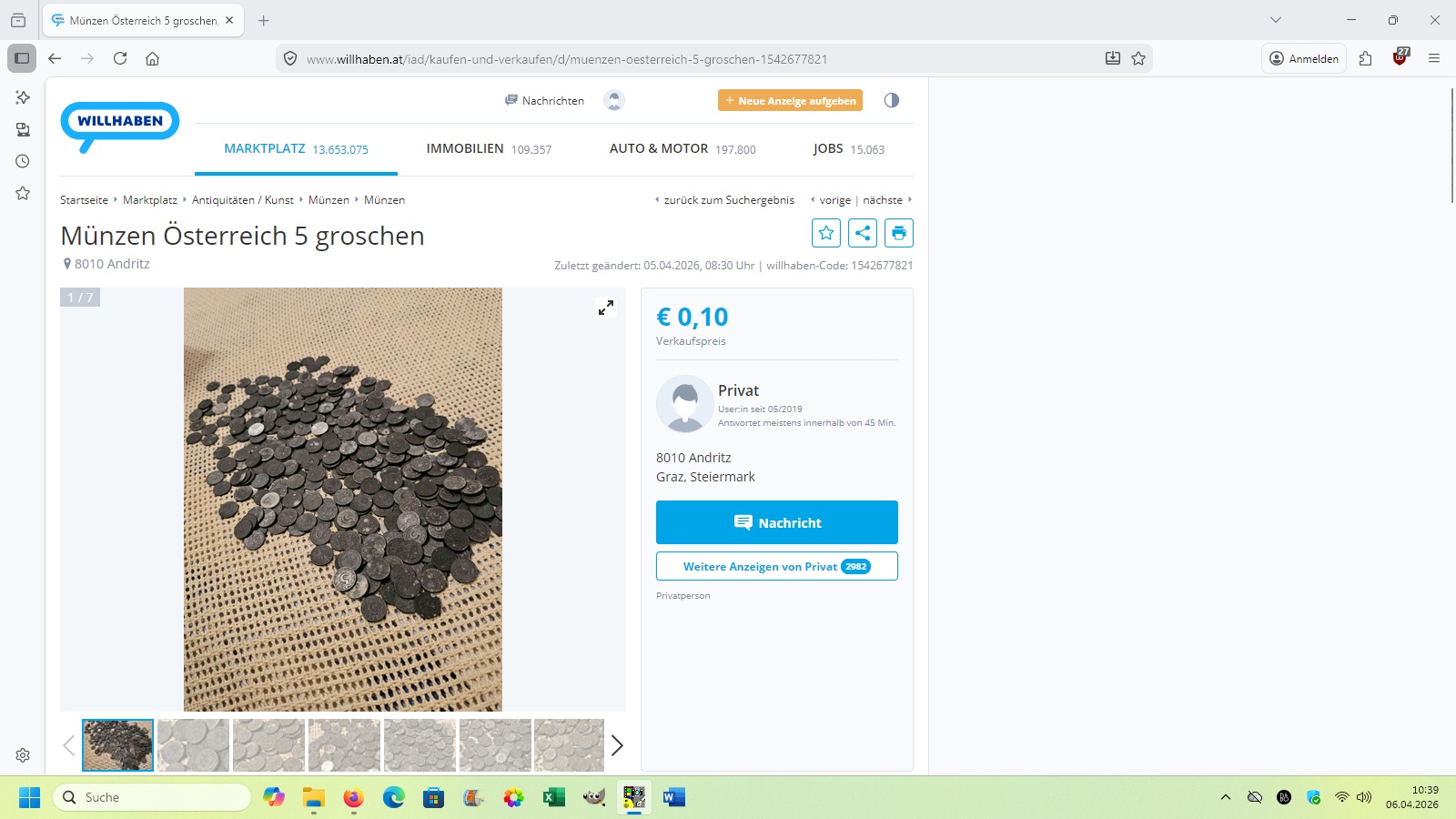


Die alten Münzen aus Österreich sind fast alle mit einer dunklen Zinkoxidschicht überzogen. Diese muss man für dieses Experiment entfernen, zum Beispiel mit Zitronensäure. Nach etlichen Stunden in der Säure hellen die Zinkmünzen zusehends auf:




Als Elektrolyt kommt bei mir Apfelessig zum Einsatz:


Löschpapier tränke ich sodann im Essig und gebe die kleinen, nassen Plättchen zwischen die Münzen:

Hier die 2-cent-Kupfermünzen…

…und die erhellten 5 Groschen Münzen:

Meine Abfolge: Kupfermünze – Essiglöschpapier – Zinkmünze – Kupfermünze usw.

Insgesamt stapelte ich 12 Elemente übereinander:


Jetzt kam der spannende Teil, würde das Voltmeter eine Spannung anzeigen?


Voila, ganze 10.73 Volt waren abzulesen…


Damit betrug die Spannung eines einzelnen Elements 10.73 / 12 = 0.89 V. Im Idealfall sollte ein jedes Kupfer-Zink-Paar eine Spannung von 1,10 V erzeugen.
Zum Schluss noch der LED-Test, natürlich mit Vorwiderstand:



Zum Schluss noch das Youtube-Short zum Experiment:

