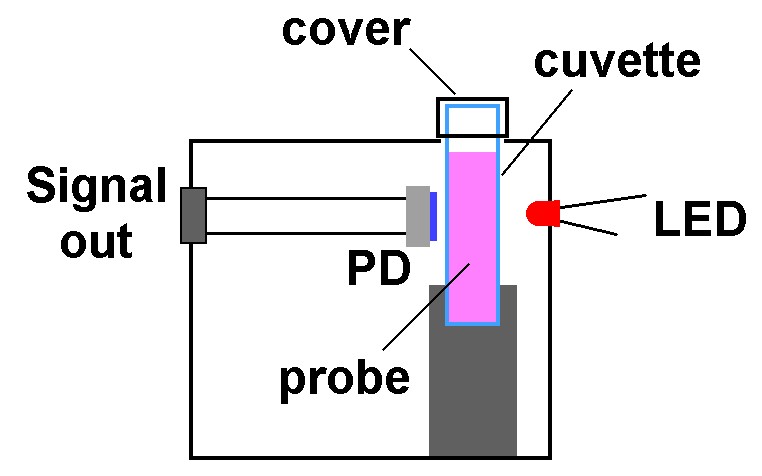
Mit einem Photometer kann die (wellenlängenabhängige) Absorption von Licht in einer Flüssigkeit bzw. Festkörper bestimmt werden. Hierzu misst man lediglich die Transmission I0 nur mit Wasser und dann die Transmission I mit der zu untersuchenden Flüssigkeit.
Variante 1: Bestimmung des Absorptionsspektrums
Für die Transmission T ergibt sich dann einfach T = I/I0 · 100 (in Prozent) bzw. für die Absorption A = 100 – T. Wiederholt man diese Messung mit verschiedenen Lichtquellen (in meinem Fall LEDs), so kann ein richtiges Absorptionsspektrum aufgenommen werden.
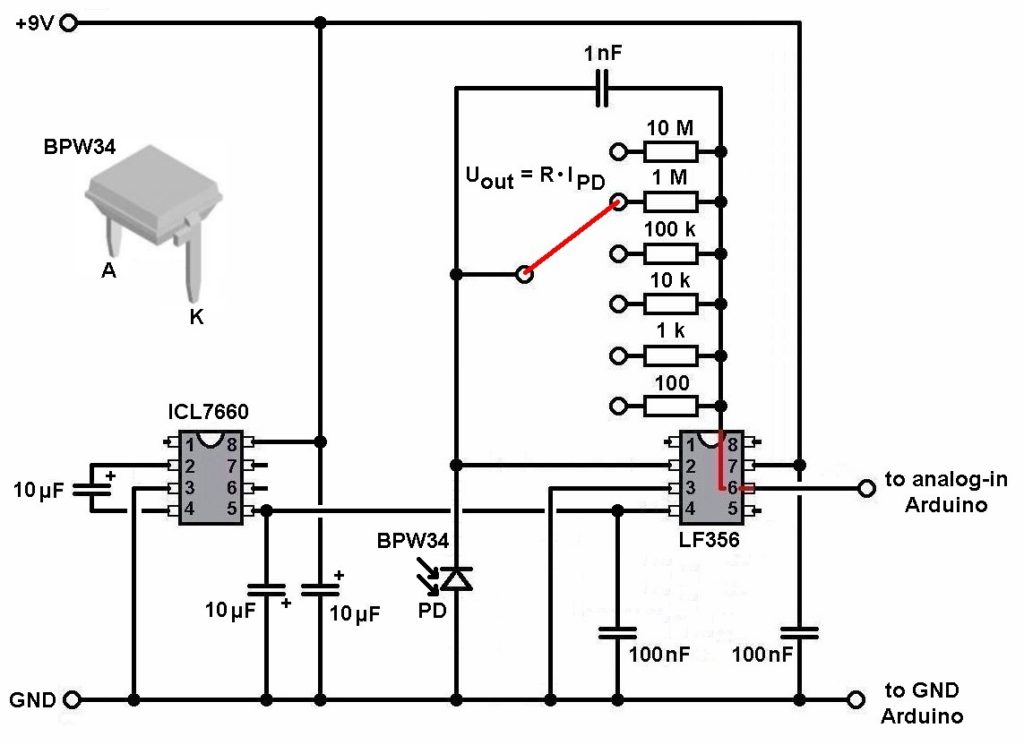
Die Intensitäten werden mit einer Photodiode (BPW34) und eines sog. Transimpedanzverstärkers (= Strom-Spannungs-Wandler) gemessen. Die Verstärkung ist über einen Drehschalter einstellbar. Die Ausgangsspannung des TIV wird mit einem Arduino eingelesen und am 16×2 I2C display angezeigt.
Um den Spektralbereich möglichst gleichmäßig abzudecken, habe ich bei der Firma Roithner in Österreich ausgewählte LEDs bestellt. Mit diesen erfasse ich Wellenlängen im Bereich [395 nm, 850 nm].
Als Testflüssigkeit eignet sich sehr gut Chlorophyll. Wie man anhand des erhaltenen Absorptionspektrums erkennen kann, absorbiert Chlorophyll stark im blauen und roten Spektralbereich. Im grün/gelben Spektralbereich ist hingegen die Transmission groß. Dies ist ja auch anhand der Flüssigkeitsfarbe (grün-gelb) zu erwarten.
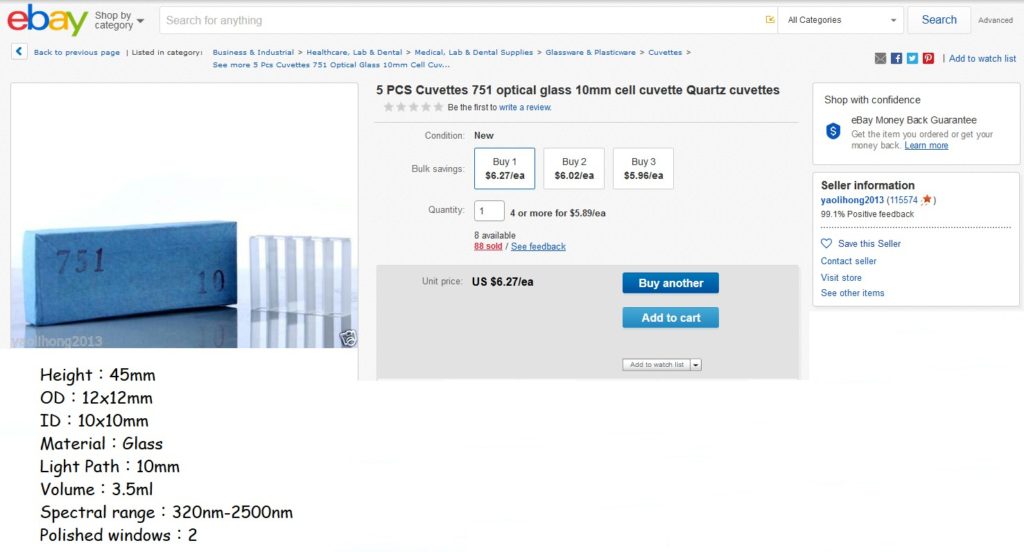



















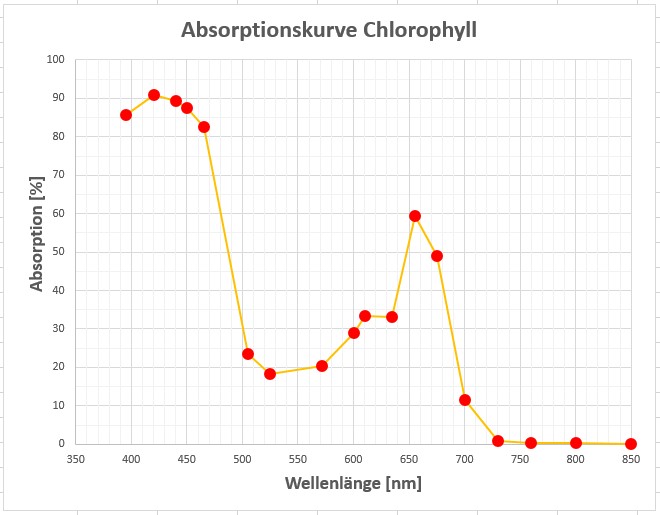
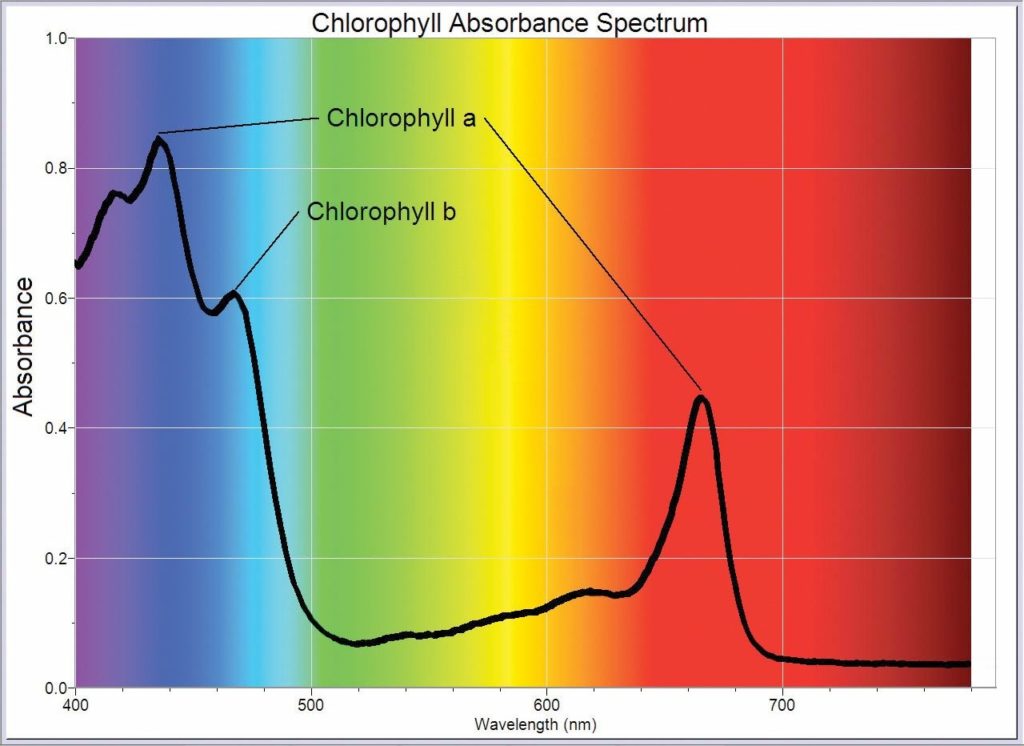
Bildquelle: https://www.vernier.com/zoom/?id=89450
Variante 2: Bestimmung der Konzentration eines gelösten Stoffes
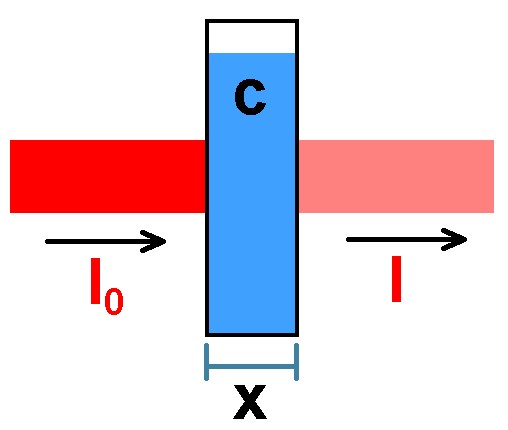
Das Lambert-Beersche Abschwächungsgesetz lautet: I = I0 · exp(–k · c · x)
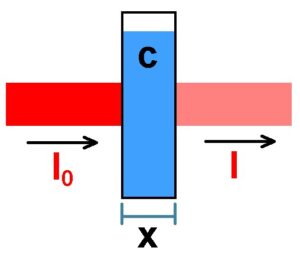
Hierin ist k eine Konstante (der sog.Extinktionskoeffizient), c die Konzentration des gelösten Stoffes und x die Länge der Probe. Als Extinktion E ist definiert: E = log10(I0/I) = log10(e) · k · c · x.
Ist etwa E = 1, so beträgt die Transmission 10^–1 = 0.1 = 10%. Bei E = 2 nur noch 1/100. usw.
Ändert man nur die Konzentration des gelösten Stoffes, so ist die gemessene Extinktion direkt proportional zur Konzentration c. Zur Eichung löst man eine bekannte Menge c in Wasser und bestimmt E. Daraus lässt sich dann die Gerade E = k‘ · c aufstellen mit dem nun bekannten Wert für k‘. Infolge misst man nur noch die Extinktion E und ermittelt daraus die unbekannte Konzentration c. Die verwendete LED (in meinem Fall eine grüne mit der Wellenlänge 525nm) darf natürlich nicht mehr gewechselt werden!
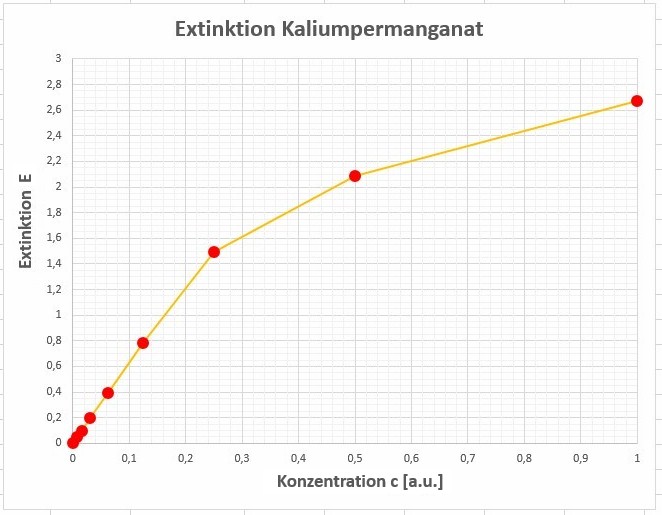
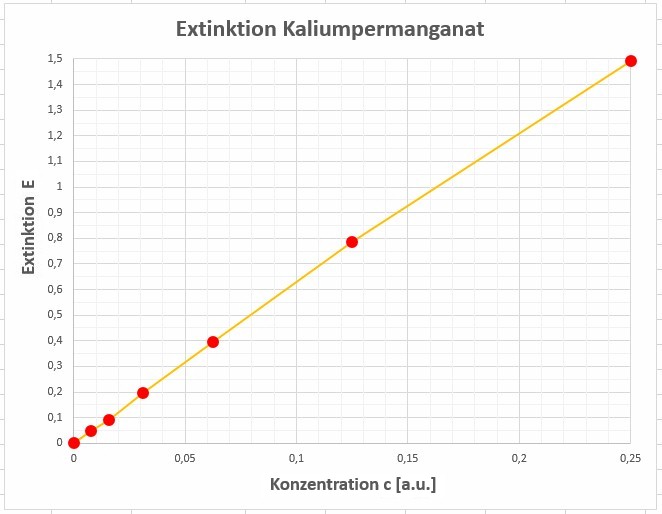
Ich habe diese Gleichung mit in Wasser gelösten Kaliumpermanganat rein qualitativ überprüft. Bei geringeren Konzentrationen erhalte ich in der Tat einen schön linearen Zusammenhang zwischen E und c. Lediglich bei hohen Konzentrationen gibt es Abweichungen.





Arduino-Code:
#include <LiquidCrystal_I2C.h>
#include <Wire.h>
LiquidCrystal_I2C lcd(0x27,16,2); // set the LCD address to 0x27 for a 16 chars and 2 line display. ACHTUNG: Adresse kann auch 0x3F sein !!!
// Anschlüsse:
// GND - GND
// VCC - 5V
// SDA - ANALOG Pin 4
// SCL - ANALOG pin 5
const int analogInPin = A6; // Analog input pin that the potentiometer is attached to
float intensity = 0; // value read from the photodiode
// ===========================
// ======= SETUP =========
// ===========================
void setup()
{
Serial.begin(9600);
lcd.begin(); // initialize the lcd
lcd.backlight();
lcd.setCursor(0,0);
lcd.print("Photometer");
lcd.setCursor(0,1);
lcd.print("Version 1.0");
delay(3000);
lcd.setCursor(0,0);
lcd.print(" ");
lcd.setCursor(0,1);
lcd.print(" ");
lcd.setCursor(0,0);
lcd.print("U_PD = ");
}
// ===========================
// ======= LOOP =========
// ===========================
void loop()
{
intensity = analogRead(analogInPin);
intensity = (intensity / 1023.0) * 5.0;
lcd.setCursor(7,0);
lcd.print(intensity,3);
lcd.print(" V");
delay(100);
}

