Elektrolyse nennt man einen chemischen Prozess, bei dem elektrischer Strom eine Redoxreaktion erzwingt. Sie wird beispielsweise zur Gewinnung von Metallen verwendet, oder zur Herstellung von Stoffen, deren Gewinnung durch rein chemische Prozesse teurer oder kaum möglich wäre. Beispiele wichtiger Elektrolysen sind die Gewinnung von Wasserstoff, Aluminium, Chlor und Natronlauge.
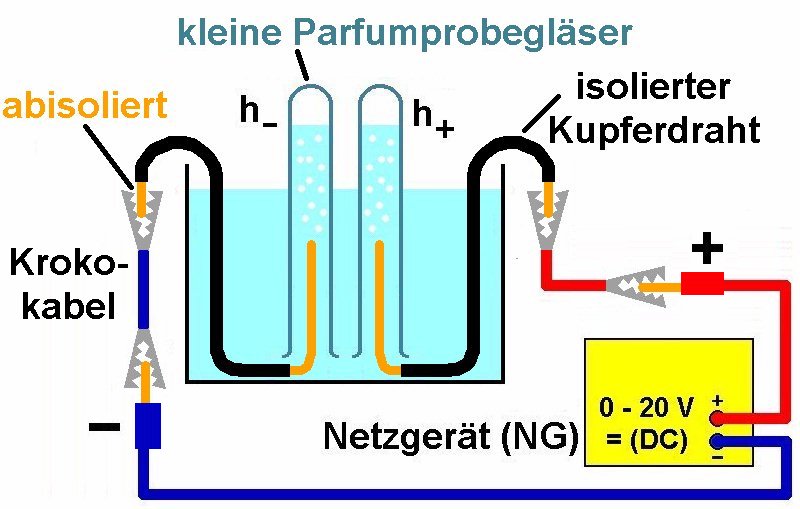
Ich werde mich hier auf die Elektrolyse von Wasser zur Erzeugung von Wasserstoff konzentrieren. Man benötigt für diesen Versuch ein Glasgefäß, ein Netzteil, Grafitelektroden, verdünnte Schwefelsäure als Elektrolyt und natürlich Wasser.



Mit reinem Wasser noch ohne Schwefelsäure ist die Menge an erzeugtem Wasserstoff sehr gering aufgrund der bescheidenen Leitfähigkeit von Wasser:



Die verdünnte Schwefelsäure (Achtung: An Privatpersonen darf nur max. 15% ige Schwefelsäure verkauft werden!) habe ich im Internet gekauft:


Die Stromstärke ist verglichen mit reinem Wasser massiv gestiegen und beträgt nun 2.5 A bei nur 4.2 V:

Mit der Schwefelsäure ist nun die entstehende Wasserstoffmenge auch deutlich erhöht:

Anhand der Reaktionsgleichung 2 H2O ⇒ 2 H2 + O2 wird klar, dass doppelt so viele Wasserstoffmoleküle erzeugt werden wie Sauerstoffmoleküle. Demnach sollte das über der Kathode entstehende Wasserstoffvolumen doppelt so groß sein wie jenes über der Anode (= Sauerstoff).
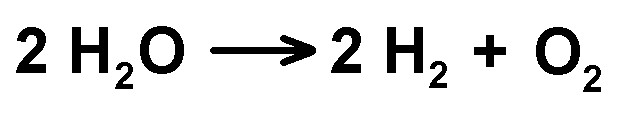
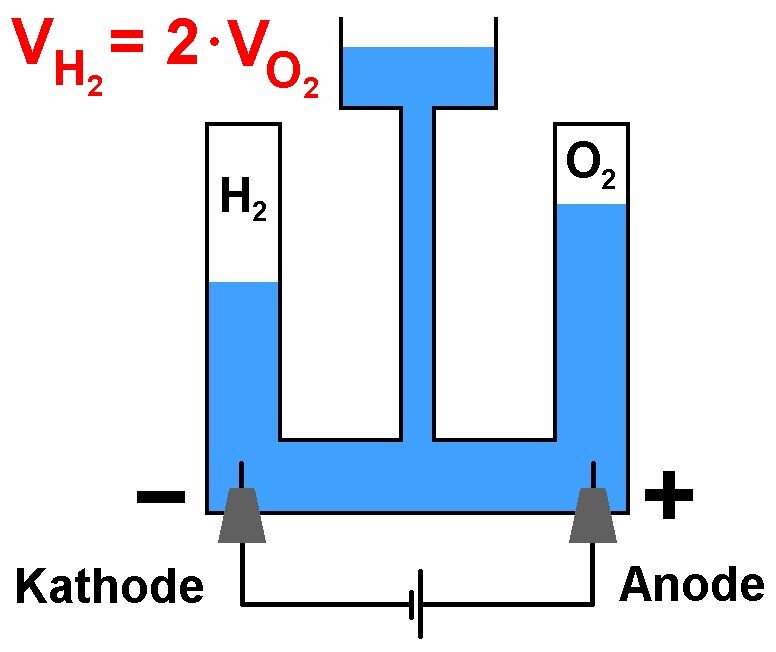
Auf Amazon bin ich auf einen extrem günstigen Wasserzersetzungsapparat nach Hofmann gestoßen. Mit diesem kann ich im Gegensatz zum ersten Aufbau im offenen Glasbehälter die entstehenden Gase sammeln, ihre Volumina vergleichen und dann z.B. zu einer Brennstoffzelle (siehe weiter unten) weiterleiten.




Mit gefüllter Schwefelsäure:


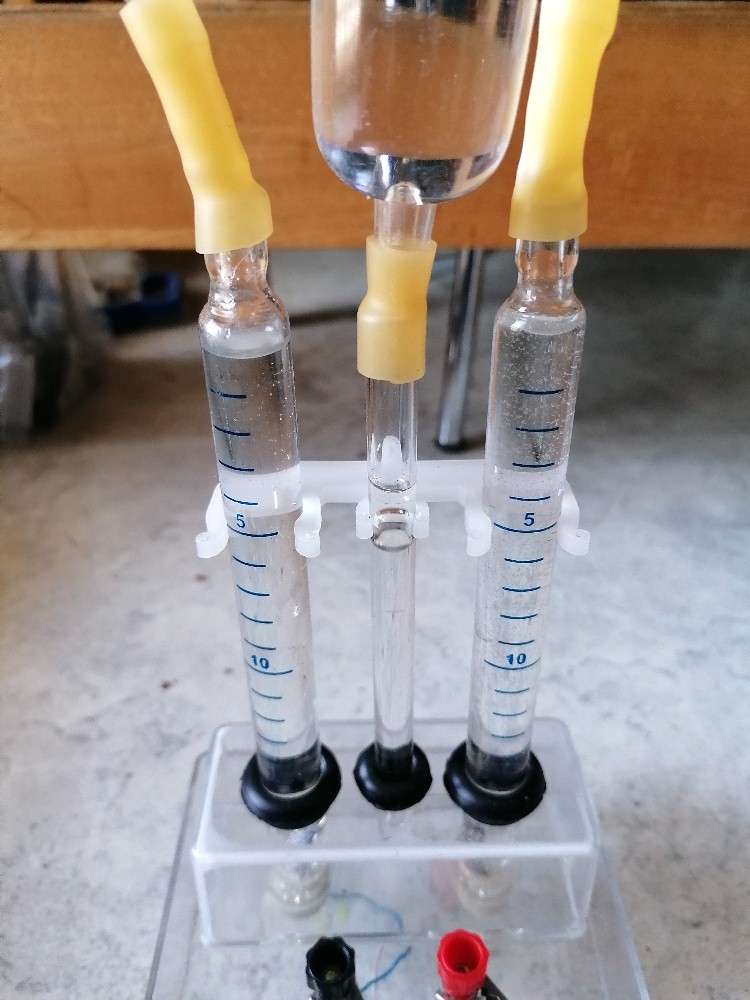
Nach Anlegen der Spannung:
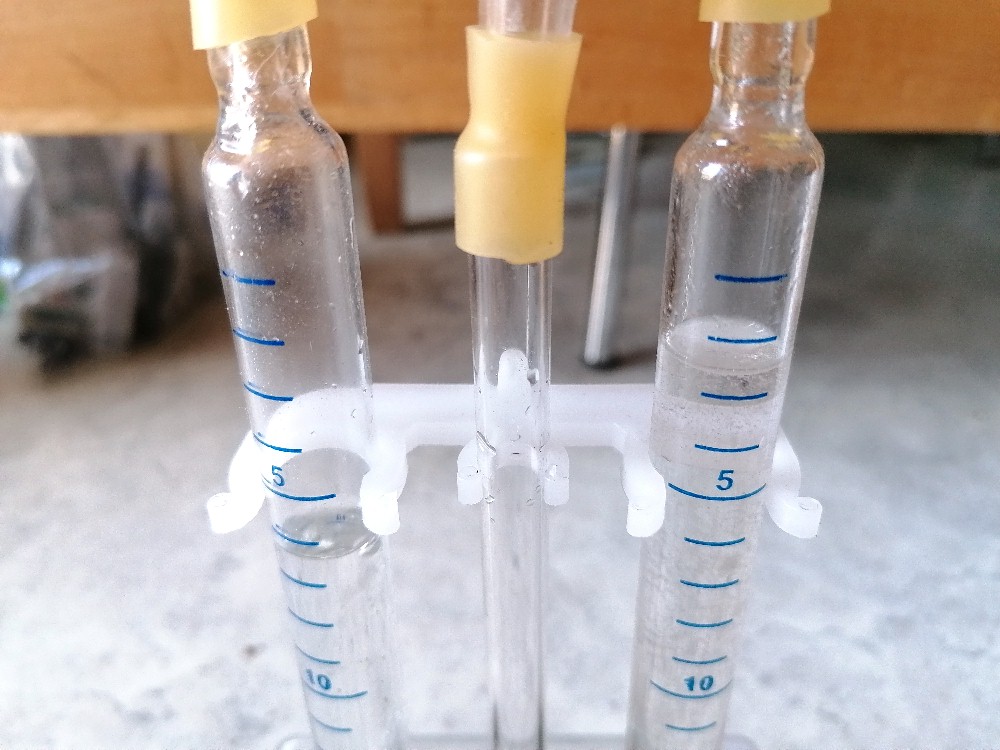
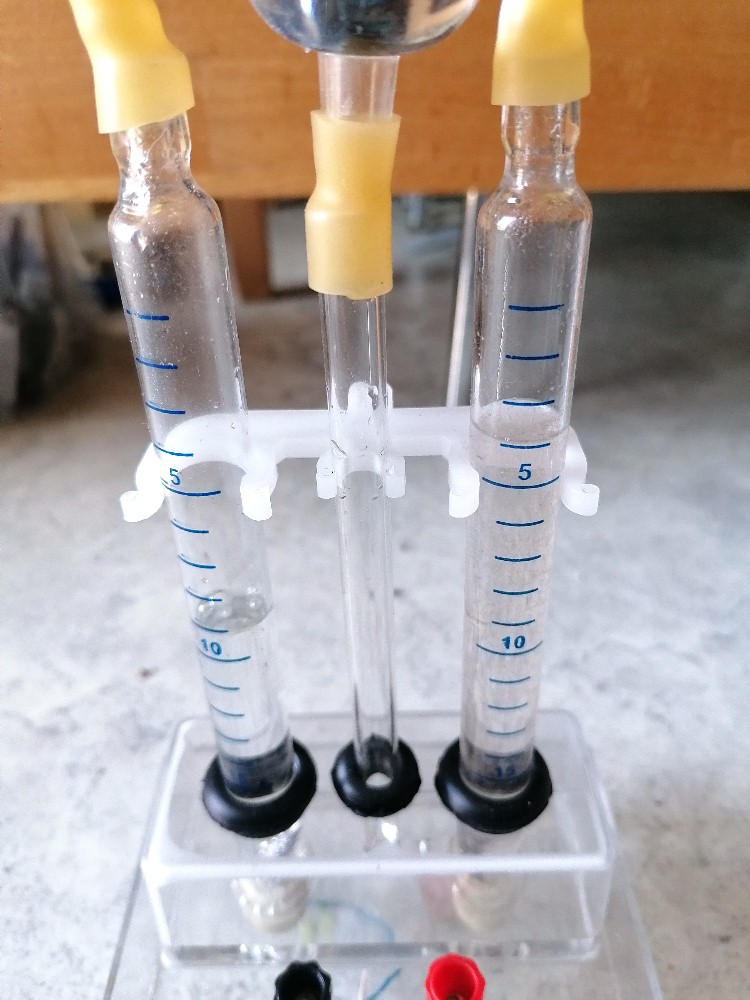
Das Sauerstoffvolumen über der Anode:

Das Wasserstoffvolumen über der Kathode:

Kann ich mit dem erzeugten Wasserstoff etwas anfangen? Ja, natürlich. Zum einen wäre da die imposante Knallgasreaktion zu nennen. Dabei entzündet man zum Beispiel einen mit Wasserstoff gefüllten Ballon an der Luft. Die imposante Explosion beeindruckt bestimmt die Schüler. Und dann kann man mit dem erzeugten Wasserstoff noch eine Brennstoffzelle betreiben.
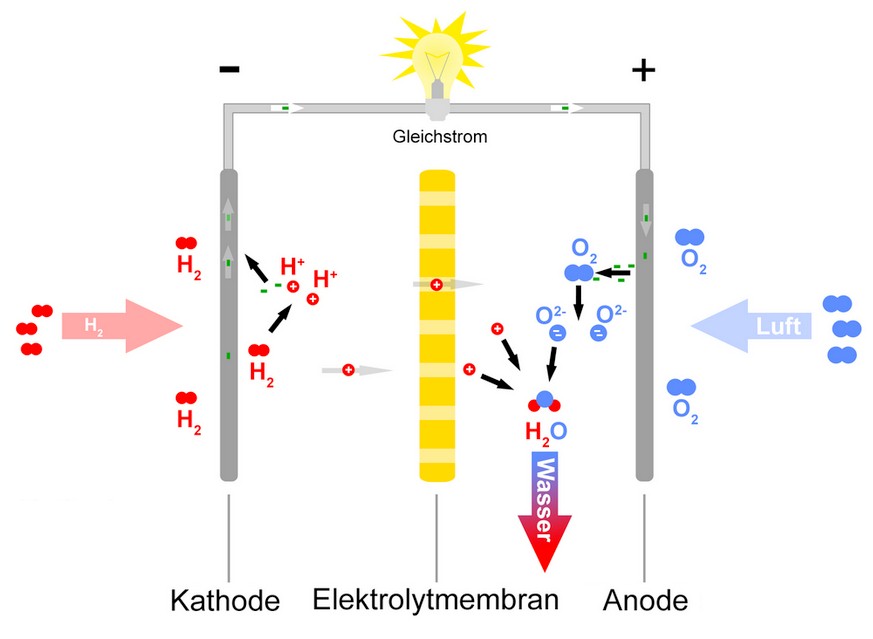
Bildquelle: Christoph Lingg, https://de.wikipedia.org/wiki/Datei:Brennstoffzelle_funktionsprinzip.png, public domain
Diese wandelt Wasserstoff und Sauerstoff in elektrische Energie um. Auf der österreichischen Verkaufsplattform http://www.willhaben.at bin ich auf ein preiswertes Angebot gestoßen:
Das Brennstoffzellen-Experimentierset ist angekommen. Der Zusammenbau war fummelig und zuguterletzt…




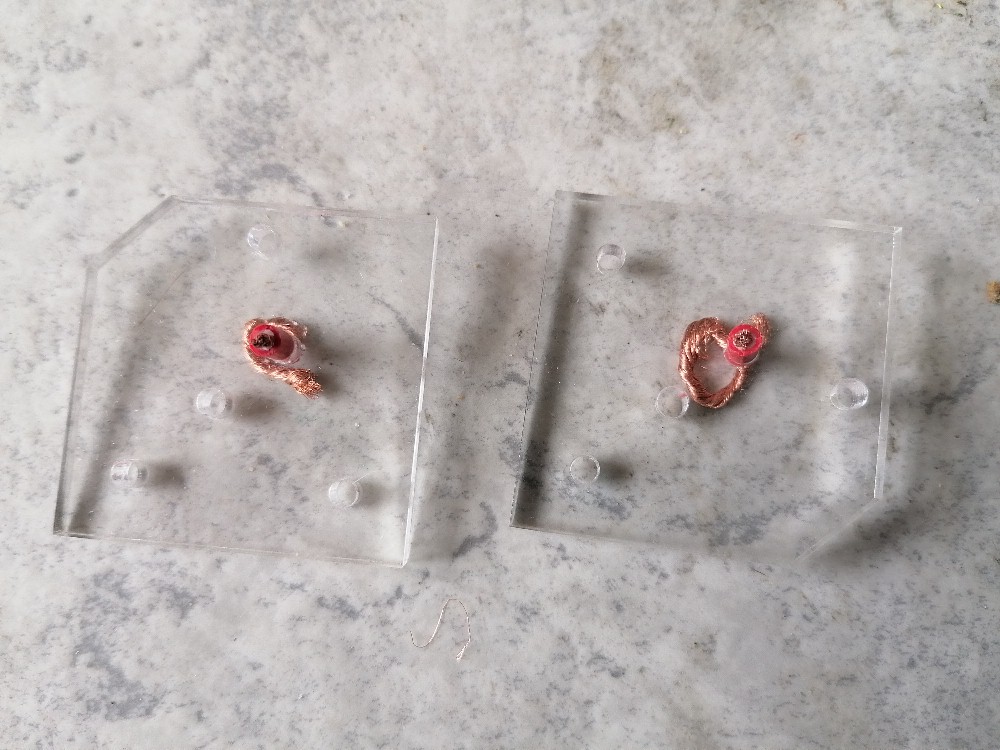
… brach mir auch noch das Plexiglas beim Anziehen der Schrauben 🙁

Mal schauen, ob ich es repariere. In der Zwischenzeit habe ich mir folgende günstige Brennstoffzelle auf Aliexpress bestellt:
Nachdem ich die auf willhaben gekaufte Brennstoffzelle nicht entsorgen wollte, habe ich sie schlußendlich repariert:




Die kleinen Schlauchtüllen zur Einleitung des Wasserstoffs:


Leider konnte ich mit der reparierten Brennstoffzelle nach Zufuhr von Wasserstoff keinerlei Spannung messen. Also war ich auf jene von aliexpress angewiesen:



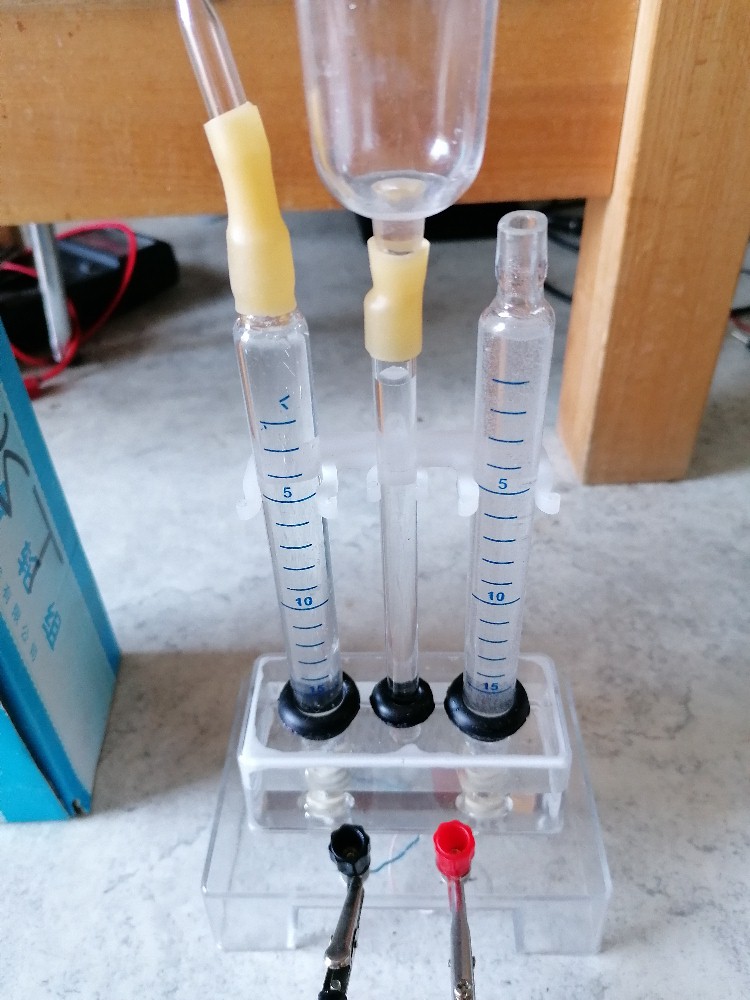


Das Voltmeter zeigte eine Spannung von über 0.8 V an:

Diese niedrige Spannung reichte aus, um einen kleinen Elektromotor anzutreiben:



