Gestoßen bin ich auf dieses Thema durch einen Jugend-forscht-Artikel (https://www.jugend-forscht.de/projektdatenbank/quantenpunkte-aus-der-kueche.html):

Quelle: jugend-forscht.de
Was sind überhaupt Quantenpunkte? Dazu ein Ausschnitt aus Wikipedia:
Ein Quantenpunkt besitzt eine nanoskopische Materialstruktur, meist aus Halbleitermaterial. Ladungsträger (Elektronen, Löcher) in einem Quantenpunkt sind in ihrer Beweglichkeit in allen drei Raumrichtungen so weit eingeschränkt, dass ihre Energie nicht mehr kontinuierliche, sondern nur noch diskrete Werte annehmen kann, wodurch Quantenpunkte mit einzelnen Atomen vergleichbare Quanteneffekte zeigen. Das Spektrum eines Quantenpunkts gleicht also dem eines Atoms, allerdings können beispielsweise Form, Größe und Zusammensetzung von Quantenpunkten oder ihr Ladungszustand (Anzahl der darin gefangenen Elektronen) beeinflusst werden. Dadurch lassen sich elektronische und optische Eigenschaften von Quantenpunkten maßschneidern. Je nach Herstellungsmethode besteht ein einzelner Quantenpunkt aus etwa 104 bis 106 Atomen.
Wegen ihrer diskreten Energiespektren werden Quantenpunkte häufig auch als künstliche Atome bezeichnet, denn die Elektronen darin besitzen – genau wie in realen Atomen – quantisierte Zustände mit diskreten Energien. Der Unterschied zu natürlichen Atomen ist, dass die Energieniveaus sogar exakt durch die experimentellen Parameter einstellbar sind. Quantenpunkte aus Halbleiterkristallen sind winzige, aus nur einigen zehntausend Atomen bestehende abgegrenzte Bereiche – noch hundertmal kleiner als die derzeitigen Bauelemente der Mikroelektronik. Mit ihren Abmessungen von nur wenigen Nanometern (millionstel Millimeter) besitzen diese ultrakleinen Systeme grundlegend neue physikalische Eigenschaften. Bereits bei Zimmertemperatur wirken Quantenpunkte als Käfige für Elektronen. Darin können sich die Ladungsträger nicht mehr frei bewegen, ihre Energie ist vollständig „quantisiert“. Quanteneffekte bestimmen in solchen Nanokristallen aus Halbleitermaterial das Verhalten. Dabei zeigen sich interessante Eigenschaften im elektrischen Transport und in der Wechselwirkung mit Licht.
Übrigens, der Nobelpreis 2023 für Chemie ging an Moungi G. Bawendi vom Massachusetts Institute of Technology (MIT), Louis E. Brus von der Columbia University in New York und Alexei I. Ekimov, ehemals bei Nanocrystals Technology Inc. in New York, »für die Entdeckung und Synthese von Quantenpunkten«. Dieses Thema ist also hochaktuell.

Bildquellen: Von US Embassy Sweden – Nobel6, CC BY 2.0, https://commons.wikimedia.org/w/index.php?curid=143178436
Von Credit Line: AIP Emilio Segrè Visual Archives – https://repository.aip.org/islandora/object/nbla%3A295619, Copyrighted free use, https://commons.wikimedia.org/w/index.php?curid=138477939
By US Embassy Sweden – 4A0A1305-Enhanced-NR, CC BY 2.0, https://commons.wikimedia.org/w/index.php?curid=143178186
In diesem Experiment geht es um die Erzeugung solcher Quantenpunkten (engl. quantum dots). Man benötigt nur folgende Zutaten:
- Ameisensäure bzw. Zitronensäure
- Harnstoff
- Feinwaage
- Pipette
- Filterpapier
- Hitzebeständiges Glasgefäß
- Mikrowelle
- destilliertes Wasser
Die beiden notwendigen Chemikalien (Ameisensäure und Harnstoff) habe ich problemlos über das Internet bestellt.



Einen hitzebeständigen 50 ml Glaskolben konnte ich bei mir in der Wohnung finden:

Leider findet sich zum Jugend-forscht-Projekt keinerlei Zusatzinformation im Internet. Deshalb habe ich einmal ChatGPT nach einer konkreten Rezeptur befragt:

Für den Start wählte ich eine Mischung aus 2 g Harnstoff und 4 ml Ameisensäure:



Der Harnstoff benötigt etwas Zeit, bis er sich in der Ameisensäure aufgelöst hat:

Nach ca. 4 Minuten:

Jetzt kommt der Glaskolben in die Mikrowelle. Auf zweithöchster Stufe (Leistung unbekannt) habe ich einmal 1 Minute eingestellt:

Binnen kurzer Zeit bildete sich eine stechende, dichte Nebelsuppe aus Ameisensäure in meiner Küche:

Ich habe natürlich sofort die Balkontüre geöffnet. Sodann erhitzte ich die Lösung vorsichtig immer nur für ca. 20 Sekunden in der Mikrowelle. Nach kurzer Zeit erkannte ich erste braune, feste Rückstände im Glaskolben:

An der Kolbenwand bildeten sich kleine, kreisrunde Flecken, welche mit UV-Licht beleuchtet fluoreszierten:

Im nächsten Schritt habe ich ein wenig destilliertes Wasser in den Glaskolben gegeben und diesen geschüttelt, sodass sich die kleinen fluoreszierenden Tropfen im Wasser lösten. Danach schüttete ich alles durch einen gewöhnlichen Kaffeefilter in ein Messglas und sodann die klare, filtrierte Lösung in ein Reagenzglas:



Im Glaskolben verblieben die festen, bräunlichen Rückstände:

Jetzt verdunkelte ich die Küche und beleuchtete die Lösung im Reagenzglas neuerlich mit meiner 365 nm-UV-Taschenlampe…

… und siehe da, ich konnte ein schönes, relativ helles bläuliches Fluoreszenzlicht erblicken:


Ich werde den Versuch noch mit Zitronensäure wiederholen in der Hoffnung, eine andere Fluoreszenzfarbe zu erhalten. Diese hängt ja von der Zusammensetzung und auch entscheidend von der Größe der Quantenpunkte ab.
So, Zitronensäure im Drogeriemarkt besorgt…

Ich habe wieder 2 g Harnstoff mit 4 ml Säure vermischt und dann in die Mikrowelle gegeben. Es bildete sich dabei wieder ein Rauch, daher unbedingt gut lüften!

Dieses Mal leuchten die Quantenpunkte schön grün-gelblich. Ich habe dann in den Kolben ein wenig destilliertes Wasser gegeben, diesen geschüttelt und dann die Lösung wieder zu filtrieren versucht. Leider bleiben die brauen Inhaltstoffe nicht im Filter stecken, sodass ich keine klare Lösung erhalten habe:

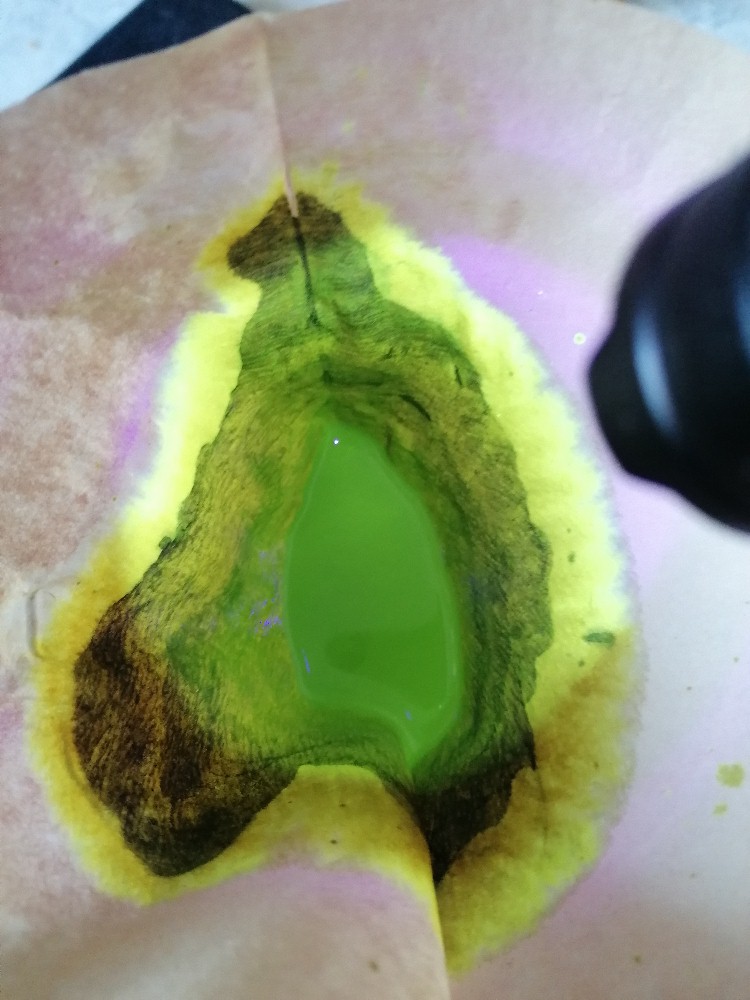

In den bereits ausgespülten Kolben gab ich dann noch einmal etwas destilliertes Wasser. Dieses löste noch einige Quantenpunkte, sodass die nun relativ klare Lösung schön gelblich fluoreszierte:


Das Youtube-Video reiche ich wie immer nach…

